原文链接:
https://www.nature.com/articles/s41467-019-09046-8
3、Cell Research:LSECtin对肿瘤相关巨噬细胞的作用通过与其受体btn3A3的相互作用而增强乳腺癌细胞的干性
巨噬细胞被认为有助于构建肿瘤干细胞(CSC)生态位。然而,人们对巨噬细胞是否以及如何通过邻分泌信号传导来调节CSC的活性知之甚少。
在这里,研究人员报告LSECtin,一种在肿瘤相关巨噬细胞(TAMs)高度表达的跨膜蛋白,增强乳腺癌细胞(BCCs)的干性。研究鉴定了BTN3A3,一种B7家族成员,具有以前未知的功能,作为BCC上LSECtin的受体,负责LSECtin的干细胞促进作用。在荷瘤小鼠体内,LSECtin的巨噬细胞特异性消融或BCC中BTN3A3的沉默降低了CSC频率和肿瘤生长。LSECtin阳性巨噬细胞的混合物增加了依赖于BTN3A3的BCC的致瘤活性。用BTN3A3-Fc或抗BTN3A3 mAb破坏LSECtin-BTN3A3轴对乳腺癌具有治疗效果。
这些发现定义了TAM促进癌症干性的邻分泌信号机制。在CSC利基中靶向该轴可以为乳腺癌提供潜在的治疗。
原文链接:
https://www.nature.com/articles/s41422-019-0155-6
4、Nature:北京生命组学研究所贺福初,复旦大学附属中山医院樊嘉,国家蛋白质科学中心钱小红使用蛋白质组学确定了早期肝细胞癌的新治疗靶点
肝细胞癌是全球癌症死亡的第三大原因。感染乙型肝炎病毒是发展肝细胞癌的主要危险因素之一,特别是在东亚地区。虽然手术治疗可能在早期阶段有效,但发生这种癌症后的五年总生存率仅为50-70%。
在这里,研究人员使用蛋白质组学和磷酸蛋白质组学分析,发现110个与乙型肝炎病毒感染相关的临床早期肝细胞癌的成对肿瘤和非肿瘤组织。定量蛋白质组学数据突出了早期肝细胞癌的异质性:研究人员使用它来将该队列分层为亚型S-I,S-II和S-III,每种亚型具有不同的临床结果。
S-III的特点是胆固醇稳态受损,与一线手术后最低的总生存率和预后不良的风险最大有关。敲除甾醇O-酰基转移酶1(SOAT1) - 其高表达是S-III亚型特异性的特征 - 改变细胞胆固醇的分布,并有效抑制肝细胞癌的增殖和迁移。最后,基于患者来源的肝细胞癌肿瘤异种移植小鼠模型,研究人员发现用SOAS1抑制剂avasimibe治疗显著减少了具有高水平SOAT1表达的肿瘤的大小。本研究中提出的早期肝细胞癌的蛋白质组学分层,提供了对该癌症的肿瘤生物学的深入了解,并提出了针对它的个性化治疗的机会。
原文链接:
https://www.nature.com/articles/s41586-019-0987-8
5、PNAS:贺福初等发现LSECtin介导的巨噬细胞对凋亡细胞的清除促进肠炎肠道修复
死亡细胞的清除对于维持组织内环境稳定至关重要,髓质C型凝集素受体(CLR)可能显著参与凋亡细胞及其碎片的清除。在这里,研究人员报道CLR成员LSECtin在巨噬细胞上表达,它们参与凋亡细胞清除。巨噬细胞通过LSECtin的吞噬作用对肠道愈合至关重要。LSECtin的缺失促进了葡聚糖硫酸钠诱导的肠上皮细胞未修复的结肠炎。这些结果表明,巨噬细胞清除凋亡细胞可以促进肠道再生。这些发现促进了对粘膜内如何维持体内平衡的理解。
上皮屏障破坏是炎症性肠病(IBD)的主要原因之一,然而,肠上皮细胞和分子对肠上皮内稳态的调节仍未明确。在这里,研究人员表明巨噬细胞上的C型凝集素受体LSECtin(Clec4g)是防止葡聚糖硫酸钠诱导的结肠炎所必需的。在机制上,LSECtin促进巨噬细胞对凋亡细胞的清除,并以吞噬依赖的方式诱导抗炎/组织修复因子的产生,从而刺激上皮细胞增殖。LSECtin的缺失导致结肠巨噬细胞吞噬有缺陷,导致异常的促分解因子产生和肠上皮修复受损。总的来说,该研究结果表明,C型凝集素受体LSECtin介导巨噬细胞对凋亡细胞的清除有助于损伤后肠再生和粘膜屏障的维持。
原文链接:
http://www.pnas.org/content/early/2018/10/08/1804094115
6、Nature communications:贺福初/王建等揭示代谢综合征治疗的潜在靶标
代谢综合征是指一系列代谢紊乱的病理状态,包括肥胖,高血压,高脂血症,高血糖和胰岛素抵抗等。代谢综合征会增加患2型糖尿病,非酒精性脂肪性肝病(NAFLD)和心血管疾病的风险。代谢综合征的患病率正在达到流行病的程度,全球估计每年有15亿人。代谢综合征与催化活性的失调或代谢酶的表达水平相关,代谢酶在葡萄糖,脂质和蛋白质的合成和/或消耗中起重要作用。代谢酶活性受多种机制调节,包括底物浓度的变化,mRNA转录的调节,以及翻译后水平限制酶的激活或抑制。先前有实验研究了代谢酶的高响应性,节能和可逆的共价翻译后修饰(例如磷酸化,酰化和甲基化)的作用。然而,蛋白水解导致关键代谢酶转换以及泛素E3连接酶的特定作用对调节代谢酶活性的作用尚未清楚。
HMG-CoA还原酶降解蛋白(HRD1)被鉴定为E3连接酶,通过调节酵母中的限速酶HMGCR(HMG-CoA还原酶)周转来控制胆固醇的产生。随后的研究表明,HRD1在内质网(ER)相关的错误折叠/未折叠蛋白降解中发挥关键作用,并保护细胞免受ER应激诱导的细胞死亡。除了错误折叠的蛋白质底物外,还发现HRD1催化IRE1α(一种ER应激传感器)的泛素结合,以抑制细胞凋亡和控制肠干细胞的体内平衡。IRE1α下游转录因子Xbp-1已被证明可调节HRD1 mRNA转录,为ER应激反应期间HRD1-IRE1α提供了一个反馈回路。HRD1被重新命名为Synoviolin,因为它在类风湿性关节炎患者的滑膜成纤维细胞中被上调,并且其上调是由促炎细胞因子通过不同于IRE1α-Xbp-1的途径诱导的。最近有研究发现HRD1参与树突状细胞抗原呈递的免疫调节,以及T淋巴细胞和B淋巴细胞的激活。然而,HRD1的器官特异性生理和病理作用仍然尚未清楚。
研究结果:
1.在肝脏中特异性缺失HRD1的小鼠显示出增加的能量消耗并且对HFD诱导的肥胖和肝脂肪变性和胰岛素抗性具有抗性。
2.蛋白质组学分析鉴定了HRD1相互作用组,其中很大一部分包括代谢调节剂。HRD1的丧失导致ENTPD5,CPT2,RMND1和HSD17B4蛋白水平升高以及随后AMPK和AKT途径的过度活化。
3.全基因组mRNA测序显示,HRD1缺陷重新编程肝脏代谢基因表达谱,包括抑制参与糖原生成和脂肪生成的基因,并上调参与糖酵解和脂肪酸氧化的基因。
结论:
HRD1可作为肝脏代谢调节剂和肥胖,脂肪肝疾病和与代谢综合征相关的胰岛素抵抗的潜在药物靶标。
原文链接:
https://www.nature.com/articles/s41467-018-06091-7
7、Nature communications:贺福初院士Nature子刊发文,通过对蛋白质组学的分析,揭示肝脏生物钟的奥秘
哺乳动物生物钟包括下丘脑视交叉上核(SCN)内的“主钟”和身体其他组织内的“外周钟”。“主时钟”充当“乐队指挥”,通过尚未定义的途径引导“外围时钟”,使动物能够根据可预测的日常环境变化调整摄食,活动和新陈代谢。
转录因子集中在小鼠肝脏生物钟中的多元组学
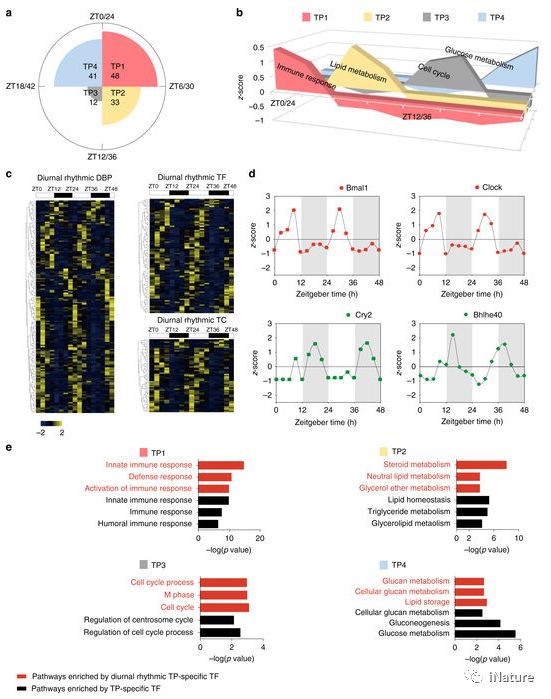
昼夜节律钟通过基因表达的时间调节来协调生理节律,以控制核心时钟基因和节奏输出程序。一个由核心转录激活因子(Bmal1和Clock)和阻遏物(Per和Cry)组成的转录 - 翻译反馈环网络,用于控制基因表达的节律性。作为特征性癌症驱动基因的Tp53和Myc以及包括Rev-erb,Ror和Ppar家族在内的几种多功能核受体(NR)也已被证明是昼夜节律钟的重要监管者。这些研究表明TFs在调节昼夜节律中的关键作用。
肝转录因子的昼夜振荡
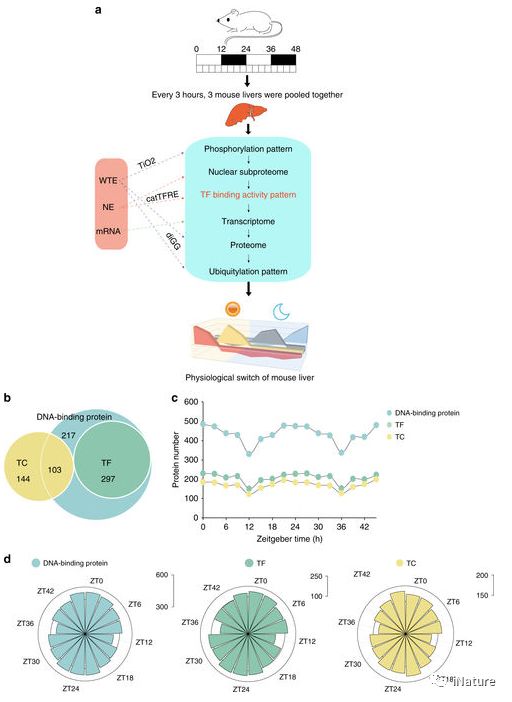
作为一个昼夜节律器官,肝脏在生物钟的不同时期执行不同的功能。这个过程被认为是由一个转录程序驱动的。在这里,研究人员提出了一个转录因子(TF)DNA结合活性为中心的多维蛋白质组学的小鼠肝脏景观,其中包括不同TFs的DNA结合谱,磷酸化和泛素化模式,核子蛋白质组,整体蛋白质组以及转录组,以描绘该组织的分层生物钟网络。
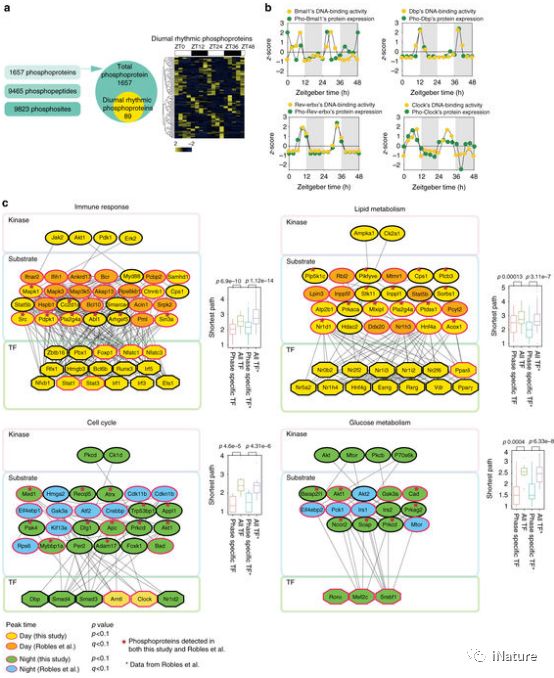
小鼠肝脏昼夜磷酸化蛋白质组
TF DNA结合活性表示四种主要途径中的昼夜振荡,即免疫应答,葡萄糖代谢,脂肪酸代谢和细胞周期。研究人员还分离小鼠肝库普弗细胞,并在昼夜节律周期中测量它们的蛋白质组,以揭示细胞型决定的生物钟。这些综合数据集为理解昼夜节律钟周围的小鼠肝脏生理提供了丰富的数据资源。
原文链接:
https://www.nature.com/articles/s41467-018-03898-2
8、Nature communications:张令强/贺福初再次出手,提供肿瘤治疗新靶标
作为基因调控最普遍的机制之一,替代剪接在蛋白质功能的复杂调控中起着至关重要的作用,剪接失调与人的癌变密切相关。AS主要由多个CIS元件来调节,这些CIS元件通过不同的机构将各种拼接因子招募到相邻的拼接位置。值得注意的是,剪接因子可分为两类,丝氨酸/精氨酸(SR)蛋白能以与环境相关的方式促进剪接,而非均质核核糖核蛋白(HnRNPs)可以正向和负调节分裂。SR蛋白由经典的SR-剪接因子(SRSF)和RNA结合的SR-样剪接因子S4组成。迄今为止,所有报道的经典SRSF敲除小鼠显示了早期胚胎致死表型,因此支持SR蛋白在体内的基本作用,并进一步表明,在不同细胞和组织条件下,SRSF的丰度和活性的微调确定剪接结果。
SRSF 5在高糖条件下稳定,促进肿瘤发生
最近的发现表明,SRSFs的失调导致多种类型的人类肿瘤的进展。例如,原癌基因SRSF 1在癌症信号通路的关键枢纽中控制着无数的基因,SRSF 2的功能增益突变有助于骨髓增殖性肿瘤的发展。此外,SRSF 9通过促进β-catenin 的积累被确认为大肠癌的致癌变压器,SRSF 10通过增强抗凋亡异构体BCLAF 1的剪接来促进大肠癌的进展。由于改变剪接可能会带来潜在的癌症风险,特别是针对SRSF的研究将为癌症治疗提供新的见解。
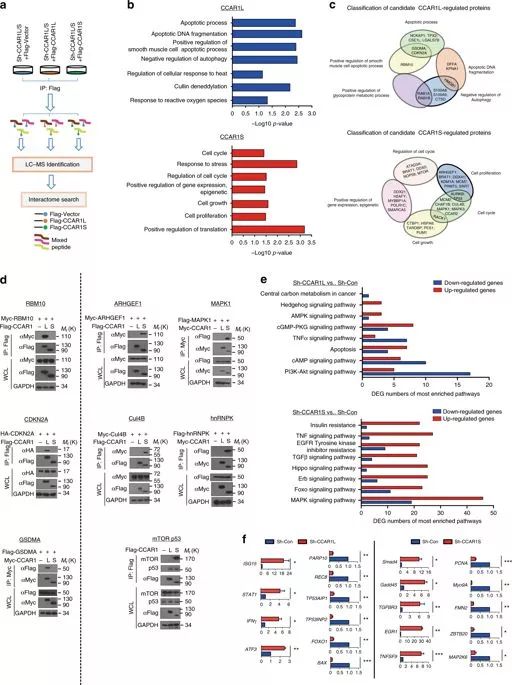
CCAR1L/S相关蛋白的网络分析
细胞代谢失调是肿瘤的标志之一,其中糖酵解途径的升高在促进肿瘤生长中起着引导作用。由于葡萄糖是最重要的营养合成来源,可以作为细胞生长的基石,因此大多数肿瘤细胞比正常细胞摄取更多的葡萄糖,细胞对高糖的反应可能是肿瘤发生的原因之一。经典的SR蛋白目前已被报道调节代谢稳态和能量依赖的发展。然而,剪接因子在糖代谢和肿瘤发展中的作用仍未明确。
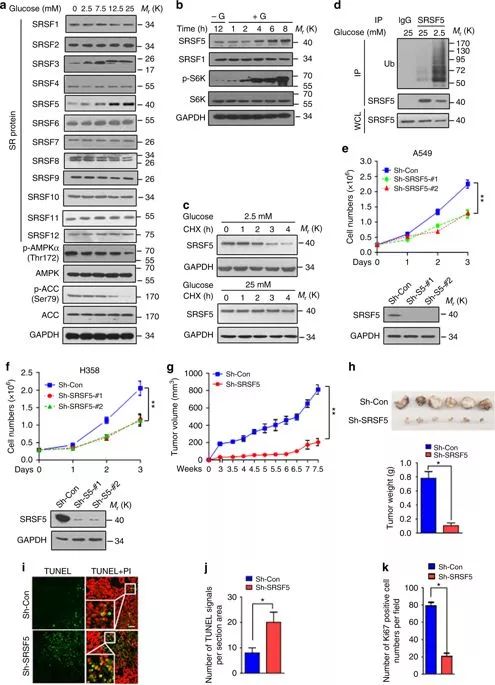
SRSF 5状态与CCAR 1剪接及肿瘤发生相关
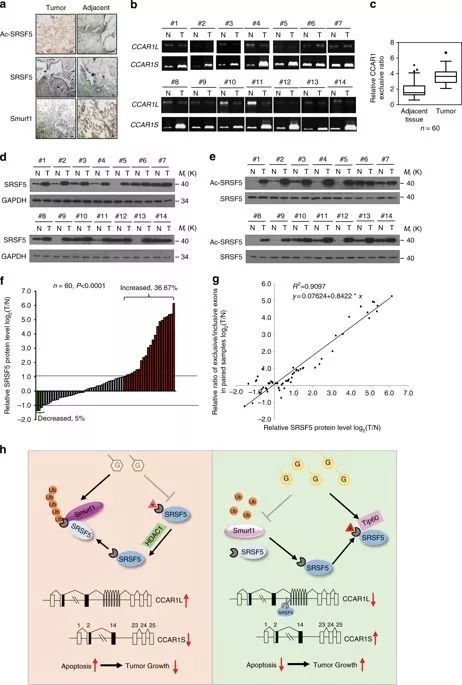
在此,研究人员发现,在葡萄糖摄入时,剪接因子SRSF 5是通过Tip 60介导的K 125乙酰化特异性诱导的,拮抗Smurf 1介导的泛素化。SRSF 5促进CCAR 1的选择性剪接,产生CCAR1S蛋白,通过增加葡萄糖消耗和乙酰辅酶A的产生促进肿瘤的生长。相反,在葡萄糖饥饿时,SRSF 5被HDAC 1去乙酰化,Smurf 1在同一赖氨酸上泛素化,导致SRSF 5的蛋白酶体降解。CCAR1L蛋白积累促进细胞凋亡。重要的是,SRSF 5在人肺癌中是高乙酰化和上调的,这与CCAR1S的表达增加和肿瘤的进展有关。因此,SRSF 5对高糖有促进肿瘤发展的作用,SRSF5-CCAR 1轴可能是肿瘤治疗的重要靶点。
原文链接:
https://www.nature.com/articles/s41467-018-04815-3